
2025-04-08 11:20:56
《中國eCTD驗證實踐手冊》作為2025年2月發布的技術指南(發布日期見),為藥品注冊申請人提供了系統化的eCTD申報驗證操作指引。該手冊基于《中國eCTD驗證標準V1.0》的框架,重點覆蓋驗證流程中的六大關鍵領域:基礎識別、文件/文件夾規范、ICH骨架文件完整性、區域性管理信息校驗、研究標簽文件(STF)邏輯性及PDF技術合規性。手冊特別強調對"錯誤警告提示"三級驗證結果的差異化處理策略,指導申請人通過賦悅eCTD軟件進行元數據填報、STF節點配置及擴展節點合規性檢查,同時針對中國特有的注冊類型差異提出模塊化申報資料準備方案。對于PDF文檔,手冊細化到書簽路徑、超鏈接屬性及字體嵌入等技術細節,確保電子資料符合CDE審評系統的解析要求。此外,手冊還結合生物制品與化學藥品的申報差異,明確了3.2.R擴展節點的使用限制,并通過案例解析說明函與申請表生命周期的管理規則。加拿大eCTD申報軟件相關技術支持。安徽賦悅科技eCTD性價比

澳大利亞的藥品電子通用技術文檔(eCTD)注冊申報體系是澳大利亞y藥品商品管理局(TGA)推動藥品審評現代化的重要舉措。eCTD作為國際通行的電子化注冊申報標準,通過結構化數據格式(如XML)整合了藥品質量、**性和有效性的技術文檔,實現了從傳統紙質遞交向數字化流程的轉型。根據TGA要求,eCTD需遵循通用技術文檔(CTD)框架,分為五個模塊:模塊1包含澳洲特定的**信息(如產品說明書草案和GMP證明);模塊2為質量、非臨床及臨床研究的綜述與總結;模塊3至模塊5則分別涵蓋藥學、非臨床和臨床的詳細數據。澳大利亞自2024年起加速推進eCTD實施,要求創新藥注冊申報優先采用該格式,以提升審評效率并支持全球同步申報。 申報流程上,企業需通過TGA指定的電子提交門戶(如eSubmission Gateway)上傳eCTD序列,并在受理后5個工作日內同步提交紙質版模塊1-5資料。江西eCTD報價歐盟eCTD注冊外包相關技術支持。
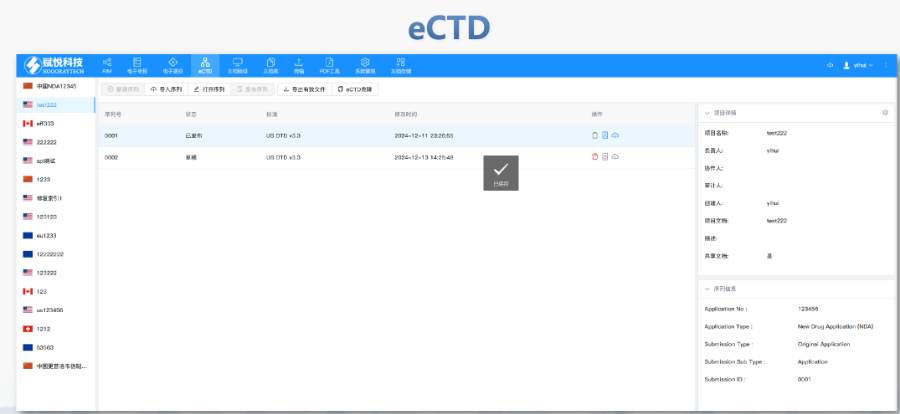
eCTD的法規框架與技術規范:歐盟eCTD的法規層級包括指南(Guidelines)、指令(Directive)和法規(Regulation)。其中,法規(如CTR)具有直接法律效力,而指南(如ICH eCTD規范)則為技術操作提供參考。eCTD的結構需符合歐盟模塊1規范(DTD 3.0+),包含**文件(模塊1)、質量數據(模塊3)及臨床研究報告(模塊5)等內容,并通過XML文件實現數據互聯。例如,CEP(歐洲藥典適用性證書)的eCTD申報需單獨構建信封(Envelope)和模塊1,并指定標識符(UUID)以確保技術合規性。
美國eCTD驗證采用三級分類:“錯誤”(必須修正)、“警告”(建議修正)、“提示信息”(參考)。例如,PDF文件版本不符或加密保護屬于“錯誤”,而書簽路徑非相對性則可能列為“警告”。驗證失敗將直接導致退審,企業需通過LORENZ Validator等工具預檢,確保提交前合規。 ?技術驗證點 驗證涵蓋XML結構合規性、文件命名規則、生命周期管理(如序列號連續性)及PDF屬性(如字體嵌入、可搜索性)。臨床試驗數據需額外滿足CDISC標準,包括SDTM和ADaM數據集的結構驗證歐盟DMF注冊申報相關技術支持。
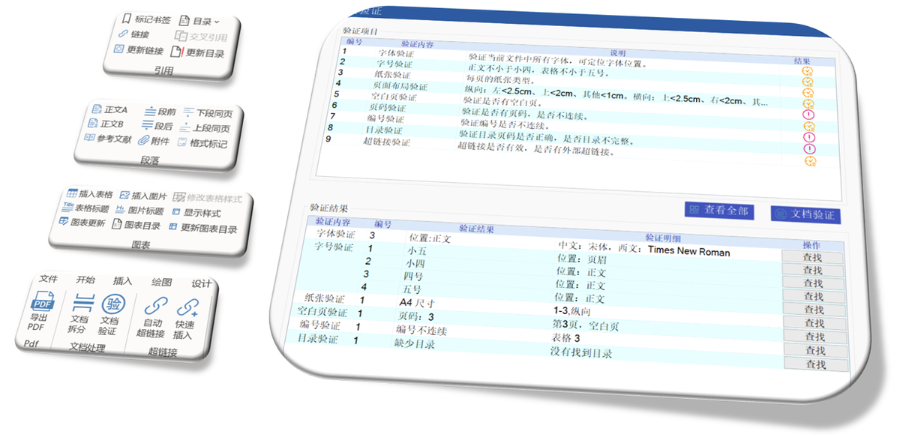
中國將進一步與國際接軌,推進eCTD等標準應用,提高藥品注冊效率和質量。AI技術可能在藥品注冊領域廣泛應用,如輔助審評人員工作。未來藥品注冊資料將更注重結構化數據,有助于監管機構高效獲取和利用數據。 eCTD等數字化工具將推動藥品監管向智慧監管和全生命周期監管發展,提高監管效率和質量。區塊鏈技術具有應用前景,可構建全球統一的藥品申報數據平臺。數據化時代,藥品注冊領域將更注重數據收集、分析和利用,為監管機構和企業提供決策支持。 總而言之,展望未來,隨著eCTD在藥品注冊領域的廣泛應用和不斷發展,中國將逐步建立起與國際接軌的藥品注冊體系。這將有助于提高中國藥品注冊的效率和質量,推動中國藥品走向世界舞臺。同時,企業也需要密切關注技術發展動態和監管政策變化,及時調整自身戰略和規劃,以適應未來的市場競爭和監管要求。澳大利亞NDA注冊申報相關技術支持。浙江中國eCTD系統
美國IND注冊申報相關技術支持。安徽賦悅科技eCTD性價比
電子簽章與傳輸** 文件需經AES-256加密后刻錄至不可擦寫光盤,并附MD5校驗碼。光盤損壞或病毒污染將觸發重遞交流程,原載體按銷毀程序處理。 ?審評與核查協同 自2018年起,FDA要求提交兩套光盤分別用于審評和現場核查,2022年調整為“1套審評+1套核查+1套專項資料”模式,提升流程效率。 ?國際化兼容性增強 美國eCTD系統支持與歐盟、日本等地區的XML互操作性,但區域差異(如模塊1的標簽要求)仍需人工適配。 ?未來通道創 FDA計劃引入API接口支持企業系統直連,并探索基于云存儲的實時提交與審評,減少物理媒介依賴。安徽賦悅科技eCTD性價比
賦悅科技(杭州)有限責任公司匯集了大量的優秀人才,集企業奇思,創經濟奇跡,一群有夢想有朝氣的團隊不斷在前進的道路上開創新天地,繪畫新藍圖,在浙江省等地區的數碼、電腦中始終保持良好的信譽,信奉著“爭取每一個客戶不容易,失去每一個用戶很簡單”的理念,市場是企業的方向,質量是企業的生命,在公司有效方針的領導下,全體上下,團結一致,共同進退,齊心協力把各方面工作做得更好,努力開創工作的新局面,公司的新高度,未來賦悅科技供應和您一起奔向更美好的未來,即使現在有一點小小的成績,也不足以驕傲,過去的種種都已成為昨日我們只有總結經驗,才能繼續上路,讓我們一起點燃新的希望,放飛新的夢想!